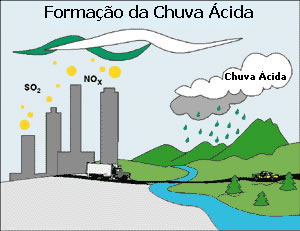
chuva ácida
A verdade é que a chuva já é naturalmente ácida devido à presença de
dióxido de carbono (CO2) na atmosfera. Com um
pH em torno de 5,4, a chuva comum não traz nenhum prejuízo ao homem ou à natureza. Isso porque, a acidez é baixa. (A escala utilizada para medir o pH vai de 0 a 14, sendo que 7 é o pH neutro. Acima disso, é básico e abaixo é ácido. Quanto mais baixo, mais ácido.) O problema, é que com a queima de
combustíveis fósseis, como o petróleo, e o aumento considerável do acúmulo de dióxido de carbono na atmosfera (além do normal) fazem com que o pH da chuva caia para algo entre 5 e 2,2 e se torne extremamente nociva ao homem e à natureza.
Robert Angus Smith (climatologista inglês) foi quem usou pela primeira vez o termo “
chuva ácida”, em 1872, ao presenciar o fenômeno em Manchester (Inglaterra) no início da revolução industrial. Foi ele, também, o primeiro a relacionar o fenômeno com a poluição atmosférica.
A chuva ácida ocorre quando existe na atmosfera um número muito grande de
enxofre (SO2) e óxidos de
nitrogênio (NO, NO2, N2O5) que, quando em contato com o hidrogênio em forma de vapor, formam ácidos como o ácido nítrico (HNO3), ou o ácido sulfúrico (H2SO4).
Estima-se, embora não haja dados concretos, que o fenômeno da chuva ácida tenha surgido com a Revolução Industrial e a crescente queima de combustíveis fósseis.
As grandes cidades como Nova York (EUA), Berlim (Alemanha) e até a Atenas (Grécia) já sofrem com os efeitos da chuva ácida há muito tempo, mas, há apenas 10 anos que este tema começou a ser investigado mais a fundo pelos ecologistas e cientistas do clima.
Os efeitos mais nocivos da chuva ácida ocorrem no meio ambiente. Um lago, por exemplo, que possui um pH em torno de 6,5 não sobrevive a um pH abaixo de 4 ou 4,5, podendo ocorrer a morte de todos os seres que vivem ali.
A chuva ácida também causa a acidificação do solo tornando-o improdutivo e mais suscetível à erosão. A acidez do solo, inclusive, é um dos principais fatores para a diminuição da cobertura vegetal em diversos países. Estudos recentes publicados pelo WWF apontam que a chuva ácida já um dos principais responsáveis pelo desmatamento na Mata Atlântica.
Para o homem o acúmulo de dióxido de enxofre no organismo pode levar à formação de ácidos no corpo humano causando até danos irreversíveis aos pulmões. Na Inglaterra, em 1952, na cidade de Londres, cerca de 4000 pessoas morreram por causa da emissão de dióxido de enxofre pela queima de carvão nas indústrias e nas casas. O pior de tudo é que nem sempre a chuva ácida cai sobre a local onde foi feita a emissão de dióxido de enxofre e óxidos de nitrogênio. Como essas substâncias estão em forma de gás, elas podem ser transportadas pelo vento por quilômetros de distância antes de cair na forma de chuva.
Formação da Chuva Ácida
 H2CO3
H2CO3